Abnorme uterine Blutung (AUB)
Inhaltsverzeichnis- Definition AUB
- Diagnostisches Vorgehen mit Fokus auf die Prämenopause
- Sarkome
- Spezielle Situationen
- Literatur
Definition AUB
Jede uterine Blutung, die nicht auf den normierten Menstruationszyklus zurückzuführen ist. Abweichungen von der Norm können Häufigkeit, Dauer, Zeitpunkt oder Menge der Blutung betreffen.
Nicht verwendete Begriffe – einige traditionelle Begriffe für abnorme Uterusblutungen (AUB) sollen nicht mehr verwendet werden, da sie verwirrend und/oder ungenau definiert sind (Menorrhagie, Metrorrhagie, Polymenorrhoe, Hypermenorrhoe, Oligomenorrhoe und dysfunktionelle Uterusblutung)
Das revidierte FIGO-AUB-System¹ ist in Abbildung 1 dargestellt, die Änderungen sind in Tabelle 1 zusammengefasst.
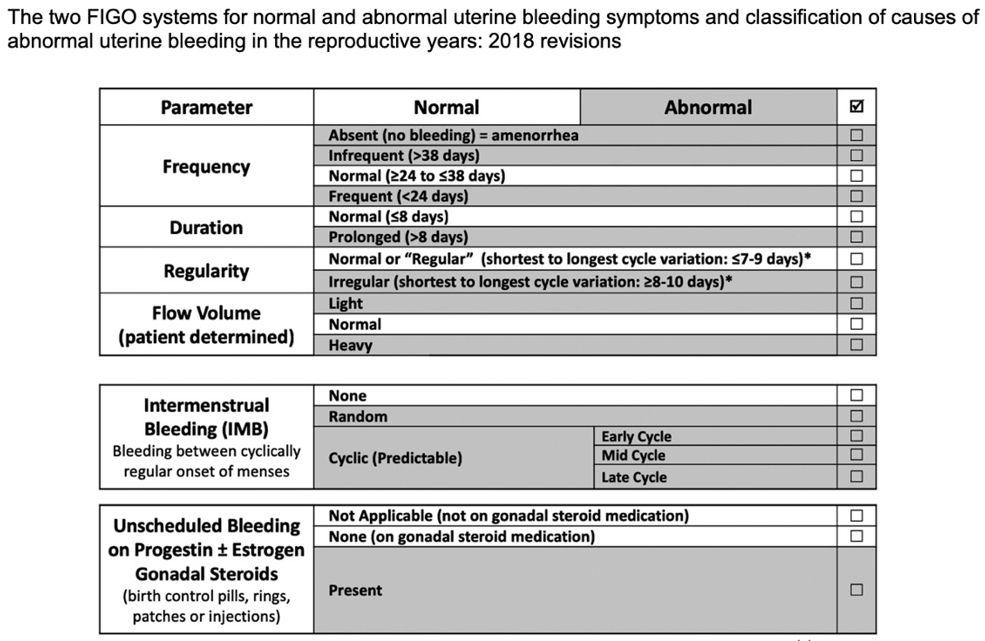
Abbildung 1
Intl J Gynecology & obste, Volume:143, Issue:3, Pages: 393-408, First Published: 10 September 2018, DOI:(10.1002/ijgo.12666)

Tabelle1
The two FIGO systems for normal and abnormal uterine bleeding symptoms and classification of causes of abnormal uterine bleeding in the reproductive years: 2018
- Chronische AUB im reproduktionsfähigen Alter - Blutung aus Uterus, die hinsichtlich Dauer, Stärke, Häufigkeit und/oder Regelmässigkeit abnormal ist und über den größten Teil der vorangegangenen sechs Monate bestanden hat.
- Akute AUB - Episode starker Blutung, die nach Einschätzung des Arztes/der Ärztin so stark ist, dass ein sofortiges Eingreifen erforderlich ist, um weiteren Blutverlust zu minimieren oder zu verhindern.
- Zwischenblutungen (Zwischenblutungen)- treten zwischen klar definierten und vorhersehbaren Menstruationszyklen auf. Diese Blutungen können unregelmässig auftreten oder sich vorhersehbar am selben Tag jedes Zyklus manifestieren.
- HMB - Symptom (keine Diagnose), der vom National Institute for Health and Clinical Excellence (in klinischen Situationen) als „übermässiger Menstruationsblutverlust, der die physische, soziale, emotionale und/oder materielle Lebensqualität einer Frau beeinträchtigt“
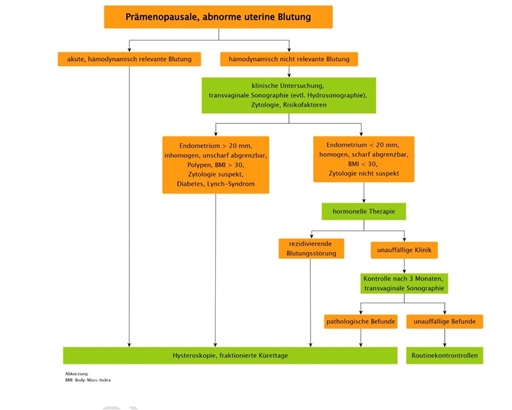
- Anamnese: gute Zyklusanamnese, Onset der Blutungsstörungen, Hinweise auf Infekt/Fieber, Trauma, GV vorangehend, mit Schmerzen bzw Dysmenorrhoe assoziiert, Hinweise auf Gerinnungsstörung, Hinweise auf weitere endokrine Störungen, Medikamenteneinnahme (Gerinnungs-beeinflussende Medikamente; Tamoxifen; Hormone); Familienanamnese
- Spekulum/ggf. Kolposkopie: Transformationszone, ev. Ektopieblutung, Tumor, Polypen/Myome in statu nascendii, ev. Pap-Entnahme, ev. Biopsie, Nativ, Abstrichentnahme
- Bimanuell: Schmerzen, Raumforderung
- Ultraschall: Hinweise auf organische Genese (Polyp, Myom, Reste nach Abort/Inter, ..); Beurteilung Endometrium nach IETA; Ovarien: PCO-like, Follikelpersistenz, and. Tumoren (solide Tumore wie Granulosazelltumore können hormonellen Einfluss auf das Endometrium haben und so zu Blutungsstörungen führen); anatomische Uterusanomalien, Hinweise auf Adenomyosis uteri
- Hydrosonographie: Bei V.a. Polyp oder intracavitäres Myom
- Zytologie/invasive Diagnostik: Tao Brush und Pipelle de Cornier
- Tao Brush zeigt die besten Ergebnisse, gefolgt von der Pipelle.
- Allerdings beide erhebliche Einschränkungen: Die Pipelle erfasst
z.B. nur einen kleinen Teil der endometrialen Oberfläche und kann fokale Veränderungen nur „zufällig“ erfassen.
Sowohl für die Pipelle als auch für den Tao Brush existiert zudem eine hohe Rate an erfolglosen Versuchen von bis zu 22 % bei Nulliparae.
- Wenn der vaginale Zugang schwierig oder unmöglich (Jugendlichen, postmenopausale Frauen), transvaginaler Ultraschall, Kontrast-Sonohysterographie und ambulante Hysteroskopie nicht durchführbar – in solchen Fällen kann eine MRT in Betracht gezogen werden. Alternativ kann eine Hysteroskopie mit indizierten Biopsien unter geeigneter Anästhesie die beste Vorgehensweise sein.
* Optimale Beurteilung des Cavum uteri 20.-25. Zyklustag (auch für Diagnostik Malformationen)
auffällig hoch prämenopausal: Kontrolle nach Menstruation
Normale maximale Werte als Orientierung (nach SGUMGG):
- prämenopausal, zyklusunabhängig: 12mm
- prämenopausal 4.-6. ZT: 5mm
zusätzliche Abklärungen (bitte situativ einsetzen, es braucht nicht immer alle):
- Labor: SST im Urin oder b-HCG im Serum; Blutbild; ev. Gerinnungsstatus; ev. kann ein orientierender Hormonstatus in gewissen Situationen helfen, bei chronischer AUB, weniger bei akuter: FSH, E2, Progesteron, Prolaktin, TSH, gesamt Testosteron, DHEAS
- HSC/Curettage: bei V.a. oder im Verlauf zum Ausschluss einer Malignität (Cave individuelle Risikoerhöhung)
- Resektoskopie bei Polypen oder intracavitären Myomen zur histologischen Sicherung falls Malignität differenzialdiagnostisch im Vordergrund
- Klassifikation PALM COEIN
Klassifikation der AUB in der Prämenopause durch FIGO, beschreibt 9 mögliche Ursachen für AUB, sie sollen bei den differenzialdiagnostischen Überlegungen helfen. Zu den PALM-Komponenten zählen strukturelle Ursachen, welche durch Bildgebung/Histologie diagnostiziert werden können, während die COEIN Komponenten die nicht-strukturell bedingten Ursachen zusammenfassen.
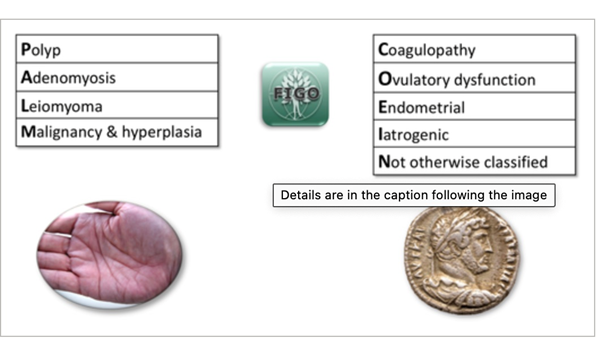
- Besteht beispielsweise der Verdacht auf eine Ovulationsstörung, ein Leiomyom Typ II und keine weiteren Anomalien, würde die Patientin im Rahmen einer vollständigen Untersuchung wie folgt kategorisiert: AUB P0 A0 L1(SM) M0 - C0 O1 E0 I0 N0.
- Da die Verwendung dieser vollständigen Notation in der klinischen Praxis als umständlich empfunden werden kann, wurde eine Abkürzungsoption entwickelt. Die abgekürzte FIGO-Bezeichnung der zuvor beschriebenen Patientin lautet AUB-LSM; -O.
AUB (P)
- Rate an malignen Polypen in prämenopausalen Patientinnen: 1.12%;
- Rate an malignen Polypen in postmenopausalen Patientinnen: 4.93% (Meta-Analyse Uglietti et al., 2019)
- Risiko von Malignität höher in symptomatischen (5.14%) als in asymptomatischen Frauen (1.89%) (Uglietti et al., 2019)
- Zu den Risikofaktoren für Malignität in Uteruspolypen zählen abnorme Uterusblutungen (AUB), höheres Alter, postmenopausaler Status, Adipositas, Diabetes, eine erhöhte Polypengrösse und die Einnahme von Tamoxifen
- Ein grösserer Polypendurchmesser korreliert mit einem erhöhten Malignitätsrisiko, während kleinere Polypen eher spontan abheilen
Therapie:
- Bei postmenopausalen Patientinnen: Hysteroskopische Polypresektion mit oder ohne Blutung
- Bei prämenopausalen Patientinnen: im Gesamtkontext beurteilen (Blutungsstörungen, Symptomatik, HCG etc.), ein Zuwarten und Kontrolle nach 1-4 Monaten postmenstruell ist meist gerechtfertigt.
- Bei störenden oder persistierenden Blutungsstörungen prämenopausal, a.e. durch den Polypen bedingt, ist ein operatives Vorgehen berechtigt; und anzustreben, wenn im Gesamtkontext (BMI, Familienanamnese (CAVE Lynch)) das Karzinom-Risiko individuell erhöht ist!
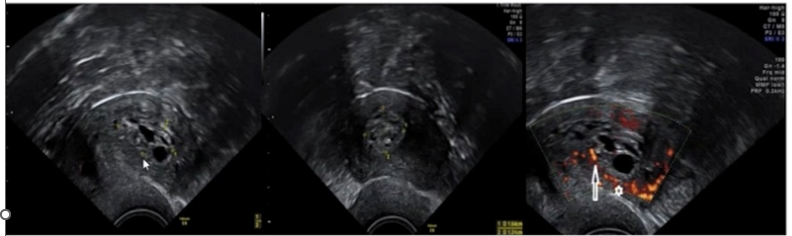
sonographische Hinweiszeichen
- ovuläre oder gelappte glatt begrenzte Raumforderungen
- homogene oder cystische Binnenstruktur
- singuläres unverzweigtes Stammgefäss
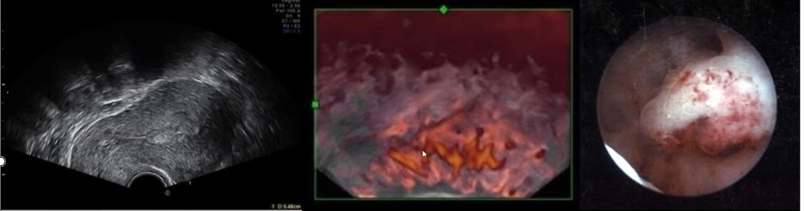
Endometriumpolyp - Malignitätskriterien
- irreguläre Berandung
- Myometriuminfiltration
- Hyperperfusion, irreguläre Gefässe
AUB (A)
The two FIGO systems for normal and abnormal uterine bleeding symptoms and classification of causes of abnormal uterine bleeding in the reproductive years: 2018 revisions
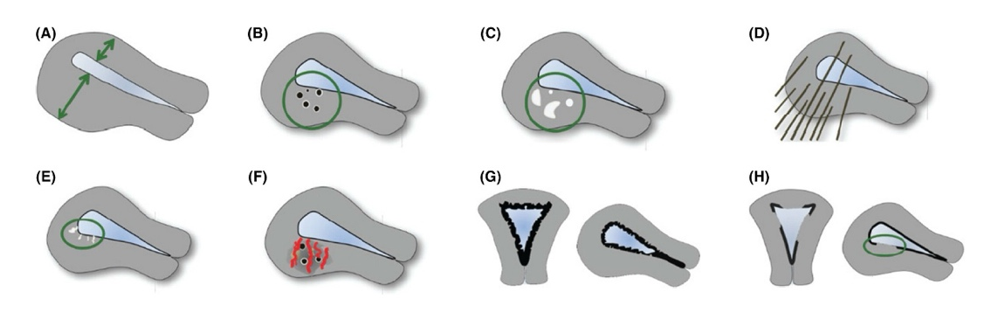
Intl J Gynecology & obste, Volume:143, Issue:3, Pages: 393-408, First Published: 10 September 2018, DOI:(10.1002/ijgo.12666)
Zumindest derzeit ist das Vorliegen von zwei oder mehr dieser Kriterien stark mit der Diagnose Adenomyose assoziiert
Therapie:
- Endokrine Endometriosetherapie oder Mirena
- Bei Therapieversagen und abgeschlossener Familienplanung: Hysterektomie
AUB (L)
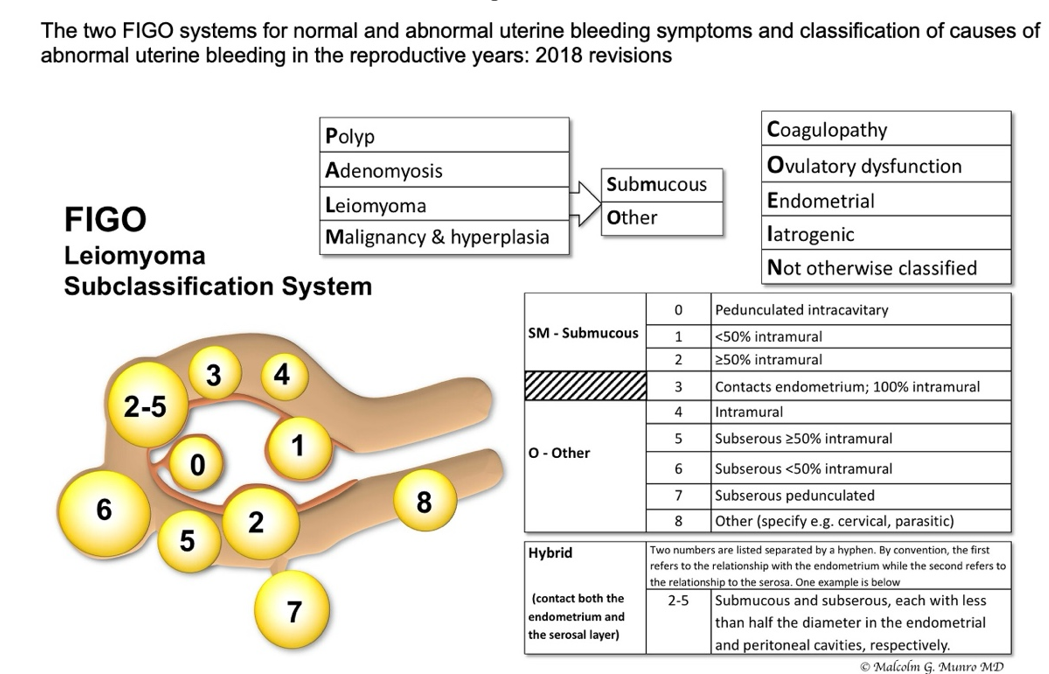
Intl J Gynecology & obste, Volume:143, Issue:3, Pages: 393-408, First Published: 10 September 2018, DOI:(10.1002/ijgo.12666)
- Die Unterscheidung zwischen Leiomyomen des Typs 0 und 1 sowie zwischen Typ 6 und 7 erfolgt nun durch Vergleich des Stieldurchmessers mit dem mittleren Durchmesser des Leiomyoms. Leiomyome des Typs 0 und 7 weisen einen Stieldurchmesser auf, der 10 % oder weniger des mittleren Durchmessers beträgt.
- Die Unterscheidung zwischen Leiomyomen des Typs 4 und 5 erfolgt anhand der Serosaverformung (Typ 5), die mittels Ultraschall oder MRT festgestellt wird.
- Beschreibung von Leiomyomen - Schätzung des Gesamtvolumens der Gebärmutter anhand von Bildgebung (transabdominaler oder transvaginaler Ultraschall oder MRT) sowie eine Schätzung der Anzahl der Leiomyome (1, 2, 3, 4 oder mehr als 4)
- die Lage (anterior, posterior, links, rechts oder zentral)
- das geschätzte Volumen von bis zu vier einzelnen Leiomyomen
- die Lage in der Vertikalen: obere Hälfte, untere Hälfte oder beides
Bei mehr als vier Leiomyomen sollte mindestens das Volumen des größten Leiomyoms dokumentiert werden.
Therapie:
- Medikamentöse Optionen: Tranexamsäure, kombinierte Kontrazeptiva, Mirena ®-IUD, GnRH-Analoga (ggf. auch präoperativer Therapieversuch, für Ryeqo® kein Kostengutsprachengesuch benötigt)
- Intrakavitäre Resektoskopie
- Myom-Embolisation bei abgeschlossener Familienplanung: Uterusmyom-Embolisation Uterine artery embolization (UAE)
- Operatives Vorgehen- v.a. bei nicht therapierbaren Blutungsstörungen, abgeschlossener Familienplanung und/oder Wunsch der Patientin: Hysterektomie
- Bei Kinderwunsch: Myomektomie
Sarkome
- Seltene Tumoren; 3% aller malignen Tumore des Uterus mit schlechter Prognose,
- Inzidenz 1.32 / 100000Frauen
- klinisch durch keine Methode voraussagbar (Pap, Curettage, Sonographie, MRI, ev. Wachstum in PMP, kein Ansprechen auf medikamentöse Therapie)
- Diagnose i. d. Regel durch Chirurgie
- Prognose (z. B. Leiomyosarkom) abhängig von Stadium
- – Medianes Überleben <5cm über 30J > 5cm 3.5J
- Verschlechterung der Prognose durch Verstreuung von Sarkomgewebe durch Morcellation bei nicht bekannten Sarkomen
- Auftreten von Leiomyosarkom, Carzinosarkom, Stromasarkome des Endometriums
- bei Morcellation 1: 350 – 1: 500; (1: 2000; Hysterektomie mit Myom)
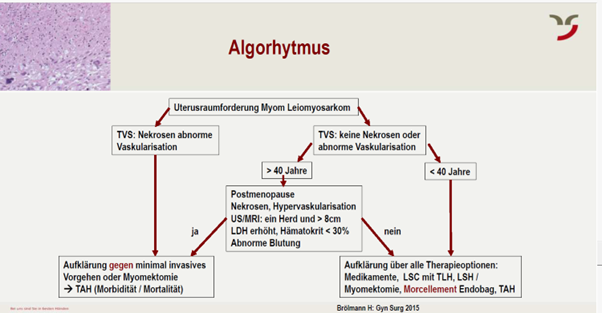
AUB (M)
- Endometriumhyperplasie bei prämenopausalen Frauen mit abnormen uterinen Blutungen liegt unter 1,5 %.
- Das führende Symptom eines EC ist die atypische vaginale Blutung.
- Da in der Prämenopause in fast 99% der Fälle den Blutungen benigne Ursachen zugrunde liegen, kann die histologische Abklärung auf Risikogruppen mit erhöhtem Risiko (Adipositas, suspekte Zytologie, Lynch Syndrom u.a.) oder auf Fälle mit suspekter Sonographie (hoch aufgebautes Endometrium >2cm, inhomogenes Binnenmuster, V.a. Invasion) beschränkt werden.
Therapie:
- Bei Frauen mit Endometriumbefunden ohne sonographische Malignitätskriterien und ohne Risikofaktoren (suspekte Zytologie, Adipositas, Lynch-Syndrom, Diabetes, Polypen) sollte zunächst ein konservativer Therapieversuch unternommen werden, sofern die Blutung nicht hämodynamisch relevant ist.
- Bei Versagen der konservativen Therapie sollte eine Hysteroskopie/Abrasio erfolgen.
AUB (C)
- Eine strukturierte Anamnese ist ein nützliches und effektives Screening-Instrument. Die FIGO empfiehlt ein Instrument mit einer nachgewiesenen Sensitivität von 90 % für den Nachweis dieser relativ häufigen Störungen (Koagulopathien).
- Bei einem positiven Screening-Ergebnis sind weitere Untersuchungen erforderlich, oft nach Konsultation eines auf Gerinnungsstörungen spezialisierten Arztes, z. B. eines Hämatologen.

Screening instrument for coagulopathies in women with the symptoms of heavy menstrual bleeding.
The two FIGO systems for normal and abnormal uterine bleeding symptoms and classification of causes of abnormal uterine bleeding in the reproductive years: 2018 revisions
AUB (O)
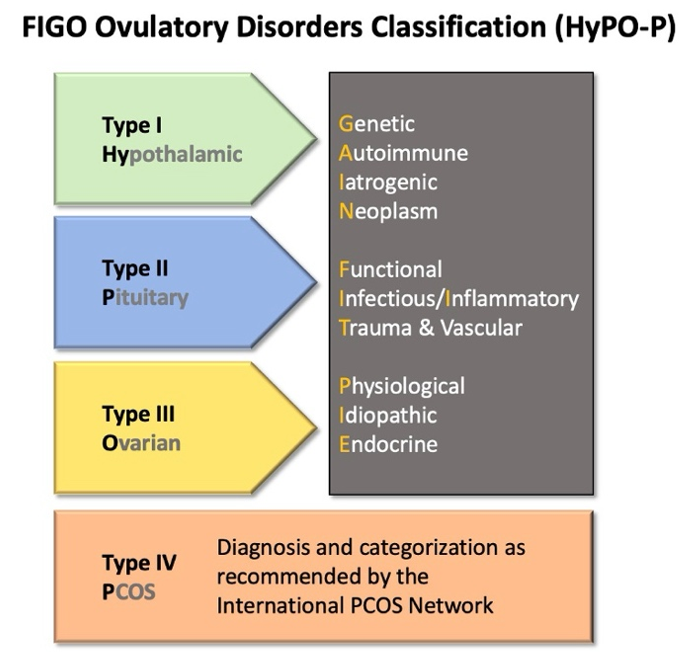
Intl J Gynecology & Obste, Volume:159, Issue:1, Pages: 1-20, First Published: 19 August 2022, DOI:(10.1002/ijgo.14331)
Therapie bei Follikelpersistenz:
- Zuwarten
- Bei hochaufgebautem Endometrium (>5mm): Primolut N ® 5mg 1-1-1 für 10 Tage mit anschliessender Abbruchblutung (Patientin unbedingt hierüber aufklären!)
- Falls rezidivierend: hormonelle Zyklusregulation (Mirena®-IUD, KOK)
AUB (N)
Die Kategorie „N“, „nicht anderweitig klassifiziert“, wurde im ursprünglichen System eingeführt, um selten auftretende oder ungenau definierte Krankheitsbilder zu erfassen. Dazu gehören unter anderem arteriovenöse Malformationen (AVM) sowie die Isthmozele (untere oder obere Zervixnische).
AUB (I)
AUB, die im Zusammenhang mit der Anwendung bestimmter systemischer Pharmakotherapien oder intrauteriner Systeme bzw. Verhütungsmittel auftritt, wird als „iatrogen“ klassifiziert.
Neben Gonadensteroiden wie Östrogenen, Gestagenen und Androgenen sowie Substanzen, die deren Produktion oder lokale Funktion direkt beeinflussen, umfasst diese Kategorie nun auch nichtsteroidale Arzneimittel, die zu Ovulationsstörungen beitragen (Phenothiazine und trizyklische Antidepressiva) sowie moderne Nicht-Vitamin-K-Antagonisten wie Rivaroxaban, das die Stärke der Menstruationsblutung stärker zu beeinflussen scheint als die traditionellen Vitamin-K-Antagonisten, wie beispielsweise Warfarin.
Spezielle Situationen
Tamoxifen und Blutungsstörungen
Die Therapie mit Tamoxifen ist ein Risikofaktor für das Auftreten von Endometriumpolypen, -hyperplasie und auch -karzinomen.
Ein sonographisches Screening des Endometriums bei asymptomatischen Patientinnen unter Tamoxifen ist trotzdem nicht indiziert.
Eine AUB bei prämenopausalen Patientinnen unter Tamoxifen muss hingegen zwingend abgeklärt werden.
Typische Phänomene des Endometriums bei Tamoxifen-Einnahme im Ultraschall sind:
- Vakuolen
- Swiss-Cheese-Phänomen
- Hoch aufgebautes, vom Myometrium schwer abgrenzbares Endometrium
Restmaterial nach Abort/Interruptio
- Sehr zurückhaltendes operatives Vorgehen, am besten abwartendes Vorgehen (mind. 4 Monate abwarten falls von Blutung tolerabel), ggf HCG-Kontrolle
- Evtl. regelmässige Blutungsauslösung mit COC in der Intervall-Einnahme
Literatur
S3 Leitlinie Endometriumkarzinom 09/2022
The two FIGO systems for normal and abnormal uterine bleeding symptoms and classification of causes of abnormal uterine bleeding in the reproductive years: 2018 revisions
Al-Mubarak, M., et al., Extended adjuvant tamoxifen for early breast cancer: a meta-analysis. PLoS One, 2014. 9(2): p. e88238.
DeMichele, A., et al., Impact of raloxifene or tamoxifen use on endometrial cancer risk: a population-based case-control study. J Clin Oncol, 2008. 26(25): p. 4151-9.
Saccardi, C., et al., Endometrial surveillance in tamoxifen users: role, timing and accuracy of hysteroscopic investigation: observational longitudinal cohort study. Endocr Relat Cancer, 2013. 20(4): p. 455-62
Braithwaite, R.S., et al., Meta-analysis of vascular and neoplastic events associated with tamoxifen. J Gen Intern Med, 2003. 18(11): p. 937-47.
Uglietti A, Buggio L, Farella M, Chiaffarino F, Dridi D, Vercellini P, Parazzini F. The risk of malignancy in uterine polyps: A systematic review and meta-analysis. Eur J Obstet Gynecol Reprod Biol. 2019; 237:48-56. doi: 10.1016/j.ejogrb.2019.04.009. Epub 2019 Apr 15.
Lee SC, Kaunitz AM, Sanchez-Ramos L, et al. The oncogenic potential of endometrial polyps: a systematic review and meta-analysis. Obstet Gynecol. 2010;116:1197–1205.
Intl. JGynecology & Obste, Volume: 159, Issue: 1, Pages: 1-20, First publishes: 19 August 2022, DOI: (10.1002)ijgo.14331
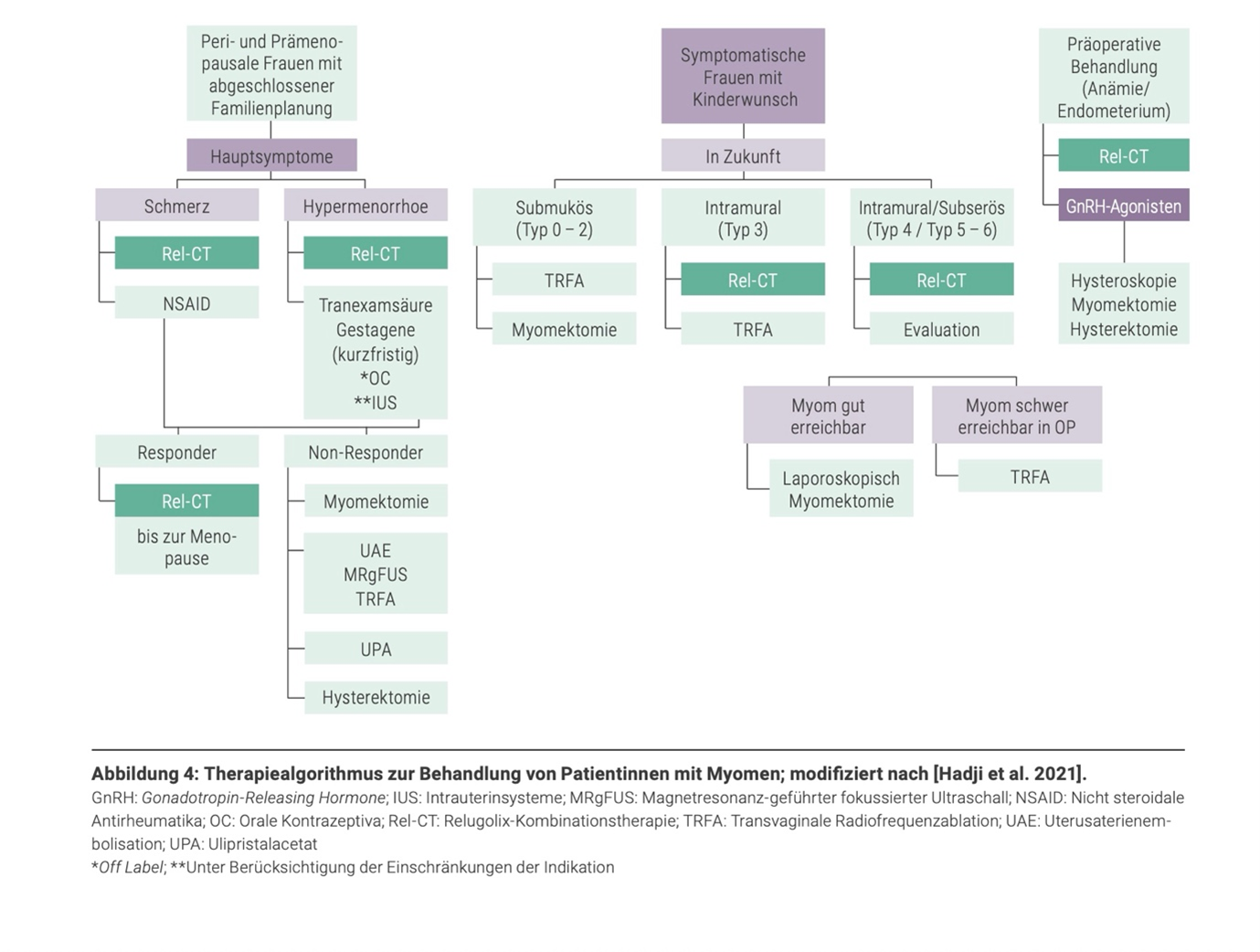
Hadj et al. 2021 Therapiealgoritmus zur Behandlung von Patientinen mit Myomen
Raspagliesi F, et al. Morcellation worsens survival outcomes in patients with undiagnosed uterine leiomyosarcomas: A retrospective MITO group study. Gynecol Oncol. 2017 Jan;144(1):90-95. doi: 10.1016/j.ygyno.2016.11.002. Epub 2016 Nov 4.
Giuntoli RL 2nd,et al. Retrospective review of 208 patients with leiomyosarcoma of the uterus: prognostic indicators, surgical management, and adjuvant therapy. Gynecol Oncol. 2003 Jun;89(3):460-9.
Leone FPG, et al. Terms, definitions and measurements to describe the sonographic features of the endometrium and intrauterine lesions: a consensus opinion from the International Endometrial Tumor Analysis (IETA) group. Ultrasound Obstet Gynecol. 2010:103–12.
Autorenschaft: M. Gellen, C. Becker
Autorisiert: S. Meili
KSW-Version: 2.0, 03/2026
